结直肠癌(CRC)作为常见的恶性肿瘤之一,其发生发展涉及复杂的基因组与表观遗传变异。以往研究多聚焦于编码基因突变(如APC、KRAS等)的驱动作用,然而超过90%的疾病相关变异位于非编码区域,提示调控元件的功能失调在肿瘤演进中扮演关键角色。增强子作为基因表达的重要调控元件,其活性受到单核苷酸多态性(SNP)和DNA甲基化等表观遗传修饰的精密调控,在肿瘤发生、转移及异质性形成中具有重要作用。尽管功能基因组学方法如MPRA等为解析非编码变异提供了工具,但由于技术限制,对结直肠癌中非编码变异及差异甲基化区域(DMR)的系统性功能注释仍然缺乏,尤其在转移性肿瘤中的调控动态尚不明确。
2026年2月20日,西北大学生命科学与医学部严健教授团队在Science Advances上发表了题为“Systematic analysis of functional genetic and epigenetic variants in colorectal cancer”的研究论文。该研究构建了一套整合性功能基因组学流程,首次在原发性与转移性结直肠癌细胞中,系统揭示了非编码SNP与CpG甲基化对增强子活性的调控网络,为理解结直肠癌的发病与转移机制提供了全新视角。

研究团队整合了SNP-STARR-seq与Methyl-STARR-seq两大高通量筛选平台,在三种结直肠癌细胞模型(原发性HCT116、SW480及转移性SW620)中,系统评估了30,790个非编码SNP与超过134,000个CpG位点对增强子活性的影响。通过这一规模化筛选,团队绘制了CRC迄今最全面的等位基因与甲基化依赖性增强子活性图谱,建立了从变异识别到机制验证的完整研究范式。
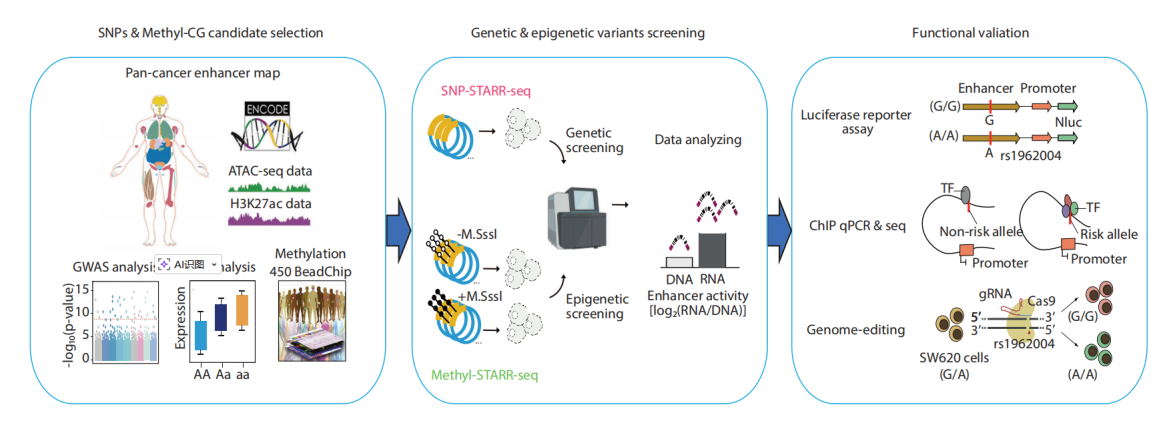
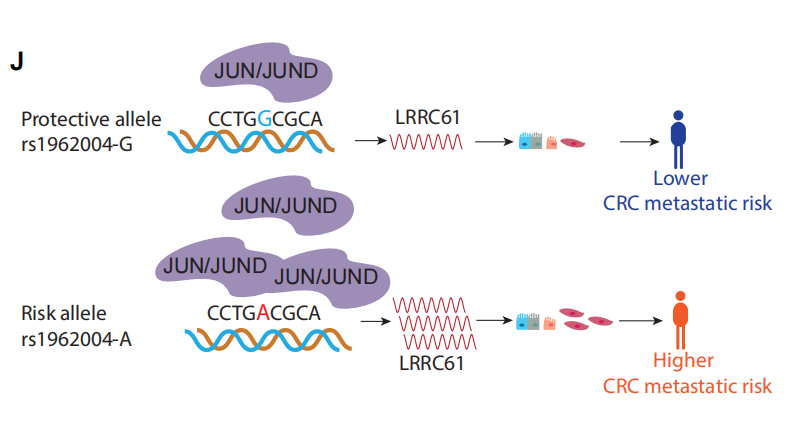
本研究在肠癌上皮细胞中鉴定出922个高可信功能性SNP,并构建这些变异可影响的转录因子及靶基因调控网络。通过对GWAS风险位点rs6061231及其连锁位点rs67941642的深入解析,研究揭示了rs67941642的T等位通过增强转录因子GFI1结合,上调抑癌基因TAF4表达,进而抑制肿瘤恶性表型的分子机制。尤为重要的是,研究利用同源配对细胞模型(SW480/SW620),首次系统识别出3,136个转移获得性SNP与3,008个转移特异性甲基化敏感元件,揭示了肿瘤转移过程中增强子序列变异调控的新机制。其中,转移获得性变异rs1962004通过招募AP-1转录因子(JUN/JUND),激活靶基因LRRC61表达,显著促进癌细胞转移并与患者不良预后相关。
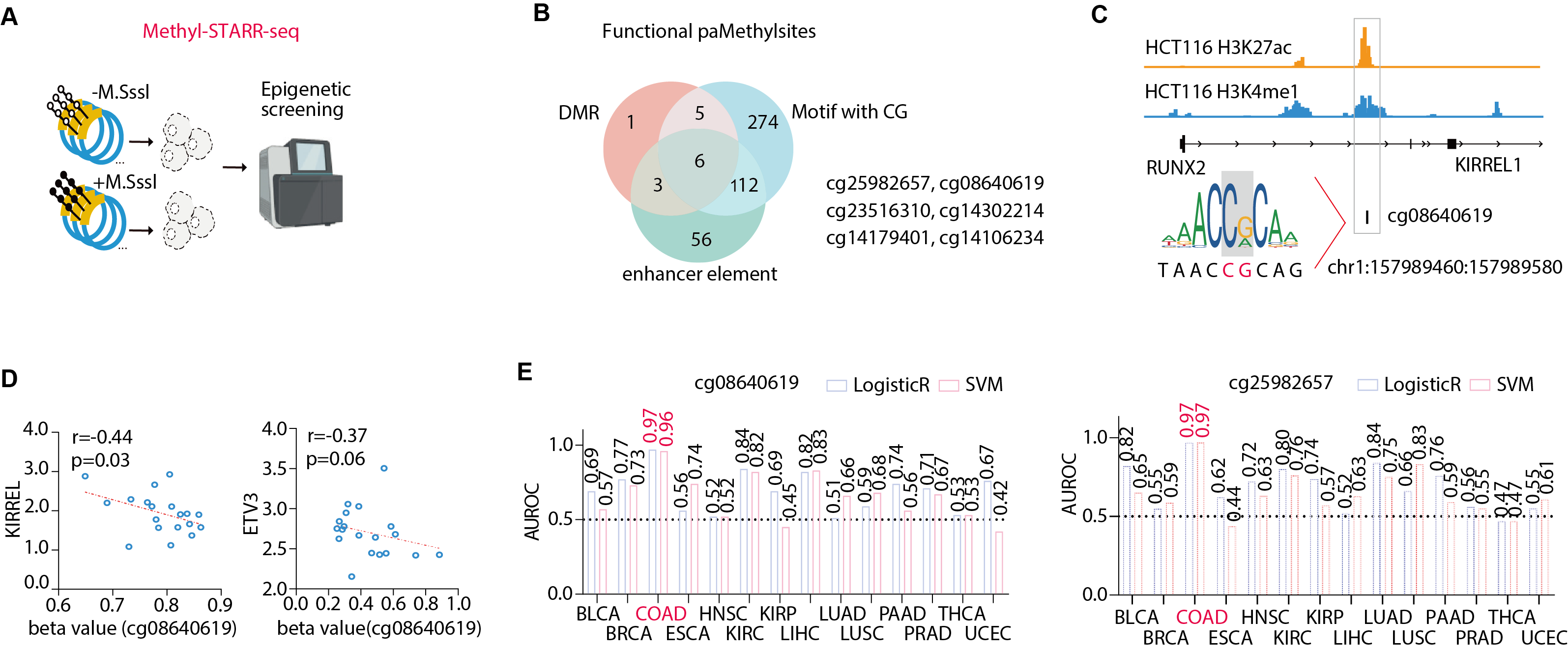
在表观遗传层面,研究结合机器学习方法,从大量CpG位点中筛选出两个具有高区分效能的甲基化标志物——cg08640619与cg25982657。其中,cg08640619的高甲基化干扰转录因子RUNX2结合,导致下游基因KIRREL1与ETV3表达下调。这两个标志物在结直肠癌早期检测中表现出极高的特异性(AUC > 0.96),展现出显著的临床转化潜力。
该研究不仅系统绘制了结直肠癌增强子区域遗传与表观遗传变异的功能图谱,更揭示了肿瘤转移过程中增强子重编程的动态机制与关键驱动力。所建立的方法体系为解析肿瘤异质性、进化转移提供了新思路,识别出的甲基化标志物也为结直肠癌的早期诊断与精准预后评估提供了新工具。
西北大学严健教授为本文唯一通讯作者,陈尔飞副教授为独立第一作者。西北大学研究生杨淇淇、戴浩洋、陈怡欣等以及医学院部分本科生也为本研究做出了重要贡献。该研究工作得到深圳市医学研究基金、国家自然科学基金、陕西省科技创新团队项目、香港研究资助局以及陕西省基础科学(化学与生物学)研究院的经费支持。
原文链接:https://www.science.org/doi/10.1126/sciadv.aeb2473